Číslo 7 - 8 / 2012
Řízená hypotermie u pacienta po KPR
ZKUŠENOSTI Z PRAXE
Souhrn: Terapeutická hypotermie prokazatelně vede ke zlepšení neurologického výsledku u pacientů po srdeční zástavě. Úkolem je dosáhnout požadované teploty 33–34 °C a výhodou je chlazení pacienta již v terénu. Je několik metod umožňujících řízenou hypotermii. Během ní je důležitá nepřetržitá monitorace pacienta a kontinuální podávní analgosedace. Hypoxie díky této metodě nemá na organismus tak devastující vliv.
Klíčová slova: kontinuální monitorování – přístroj Coolgard – terapeutická hypotermie.
(Controlled hypothermia after cardiopulmonary resuscitation)
Summary: It has been clearly established that therapeutic hypothermia leads to improved neurological outcome in patients after cardiac arrest. The challenge is to achieve the target temperature of 33 °C to 34 °C and cooling the patient already before the arrival to hospital is an important advantage. There are several methods used to induce controlled hypothermia. Continued monitoring of the patient is necessary during use of controlled hypothermia and the patient must be continuously administered analgesics and sedatives. Thanks to this method the impact of hypoxia on the organism is less devastating.
Key words: continuous monitoring – Coolgard device – therapeutic hypothermia.
Úvod
Nárůst počtu pacientů se srdeční zástavou, a tím i počet resuscitovaných, souvisí se zvýšeným výskytem civilizačních chorob. Zlepšující se postupy ze strany primární péče, jednak spektrem léků, ale také rozrůstající se sítí kardiointervenčních center, nabízejí pacientovi lepší možnosti léčby srdeční zástavy. Musíme však myslet také na časový faktor, který je stále nejzásadnějším markrem ovlivňujícím kvalitu přežití pacienta po kardiopulmonální resuscitaci (KPR). Během KPR dochází k hypoxii (nedostatek kyslíku pro tělesný metabolismus) z nedostatečného přísunu kyslíku do jednotlivých orgánů, nejcitlivější na hypoxii je mozková tkáň, dochází k odumírání mozkových buněk, které již nejsou schopné regenerace. Během srdeční zástavy dojde k centralizaci oběhu a prioritně jsou zásobovány kyslíkem buňky srdeční a buňky centrální nervové soustavy (CNS). Pokud dojde ke zničení větší části mozkové tkáně, nastává nezvratné poškození tohoto orgánu, projevující se například otokem s následujícím neurologickým poškozením. CNS reaguje na hypotermii při poklesu o jeden stupeň tělesné teploty snížením mozkového metabolismu o 6–7 %, dále klesá intrakraniální tlak (ICP), který je velmi vysoký např. při posthypoxickém edému mozku, devastujícím mozkovou tkáň utlačením. Terapeutická hypotermie všeobecně zpomalí metabolismus v celém organismu, buňky důležitých orgánů nemají takovou potřebu kyslíku, a proto se jejich tolerance zvýší. S největší pravděpodobností nedojde k poresuscitační nemoci, kterou doprovází např. ARDS (Acute Respiratory Distress Syndrome – syndrom akutní respirační tísně) nebo dokonce SIRS (Systemic Inflammatory Response Syndrome – syndrom multiorgánové dysfunkce). Podchlazení organismu – terapeutická hypotermie – je novým krokem v terapii srdeční zástavy. Z mnoha studií je zřejmé, že řízená hypotermie u pacienta po KPR je přínosem hlavně z hlediska pozdějšího neurologického nálezu, ale také jako prevence poresuscitační nemoci, která výrazně zhoršuje prognózu pacienta.
Chlazení pacienta v terénu
Během resuscitace je velmi důležitá monitorace základních životních funkcí pacienta. Monitorujeme 4svodové EKG (kontinuální sledování srdeční akce, detekce poruch srdečního rytmu), SpO2 (transkutánně měřená saturace kapilární krve), NIBP (neinvazivní krevní tlak měřený pomocí manžety) a CO2 ve vydechovaném vzduchu (měřený z ventilačního okruhu pacienta). Nezbytně nutné je sledování vědomí pacienta, nejlépe podle stupnice GCS (Glasgow Coma Scale). Po zajištění základních vitálních funkcí se přistupuje k chlazení pacienta. Nejnovější metodou je použití přístroje RhinoChill. Je to metoda používaná v přednemocniční péči (PNP) k ochlazování mozku pomocí speciálního nosního katetru. Dochází zde k odpařování perfluorohexanu, který je ve formě spreje aplikován pomocí tohoto speciálního katetru na sliznici nosohltanu a paranazálních dutin. Dochází přímo k ochlazování mozku přes bázi lební a nepřímo krevní cestou přes bohatě prokrvené okolní tkáně. Nejlépe je začít s ochlazováním ihned po zajištění dýchacích cest endotracheální rourkou (ETI) a pokračovat v něm po celou dobu transportu až do předání pacienta na příslušné oddělení, které je schopno pokračovat v terapeutické hypotermii. Výhodou tohoto přístroje je možnost snadné, rychlé a neinvazivní aplikace.
Každý sanitní vůz nemá k dispozici přístroj RhinoChill, ale může využít dalších možností. Každého resuscitovaného s teplotou nad 35 °C, s výjimkou přítomných vylučovacích kritérií, je potřeba chladit. Některé vozy záchranné služby jsou vybaveny ledničkou na infúzní roztoky. V tomto případě se podávají rychle 2 litry chladných krystaloidních roztoků a zbytek chlazených vaků se může použít na zevní obložení pacienta. Chladivé obklady se pokládají na velké cévy (ze strany na krk, do třísel atd.).
Terapeutická hypotermie v intenzivní péči
V poresuscitační péči je řízená hypotermie dnes již považována za standardní součást terapie po KPR. Nemocní po KPR by proto měli být směrováni do zdravotnického zařízení, které touto metodou disponuje.
Indikace – řízená hypotermie je indikována u nemocných po KPR nebo u nemocných s předpokladem závažné mozkové hypoperfuze; u pacientů, u nichž doba mezi časem zástavy a zahájením resuscitace (laické i odborné) není prokazatelně delší než 15 minut a přetrvává bezvědomí.
Kontraindikace – dobré vědomí (pacient vyhoví výzvě), terminální stav základního onemocnění, klinický stav, jehož závažnost s největší pravděpodobností vylučuje přežití nemocného, pacient se známým imunodeficitem, porucha koagulace s klinickými známkami závažného krvácení a bradykardie se známkami nízkého srdečního výdeje.
Přístroj Coolgard – tato endovaskulární metoda využívající speciální katetr, který je zaveden do dolní duté žíly cestou vény femoralis, je velmi efektivní. V uzavřeném okruhu proudí chladný fyziologický roztok, jehož teplota a rychlost cirkulace jsou řízeny extrakorporální jednotkou, která vyhodnocuje informace na základě teploty tělesného jádra. Tato teplota je měřena z teplotního čidla napojeného na speciální permanentní močový katetr (PMK). Způsob zavedení je totožný se zaváděním centrálního žilního katetru (CŽK), nezbytností je použití sterilního stolku a aseptický přístup jak ze strany lékaře, tak i ze strany všeobecné sestry. Tento speciální katetr je trojcestným CŽK, který má ovšem další vstup a výstup pro uzavřený okruh cirkulace chladicího média (fyziologický roztok 1/1; FR). Tento FR protéká v balóncích podél katetru, a tak dochází k tepelné výměně mezi chladným roztokem a krví.
Je důležité začít s chlazením pacienta co nejdříve, a proto při příjmu na intenzivní lůžko je prvním krokem podání chladných krystaloidních roztoků. Tím předcházíme prodlevě před zavedením katetru k přístroji Coolgard. Součástí každého přístroje je zjednodušený návod k použití a samotná příprava přístroje není složitá. Nutností je speciální set, na který napojíme FR o objemu 500 ml, přístroj Coolgard, má jednu hnací pumpu a samotná příprava nezabere více než 10 minut. S uvedenou endovaskulární metodou jsme schopni pacienta zchladit do 60 minut na cílovou tělesnou teplotu jádra 33–34 °C. Přístroj získává informace o teplotě jádra z teplotního čidla v permanentním močovém katetru a díky této zpětné vazbě je schopen reagovat na případnou změnu teploty. Coolgard udržuje nastavenou tělesnou teplotu s možnou odchylkou 0,2 °C. Teplota 33–34 °C je udržována 24 hodin.
Výhody a nevýhody metody. Největší výhodou popsané endovaskulární metody je možnost kontrolovaného ohřevu po skončení řízené hypotermie. Zahřívání lze kontrolovat nastavením přístroje, např. 0,35–0,5 °C za hodinu, na cílovou teplotu 36,5–37 °C. Doporučuje se také udržovat pacienta dalších 48 hodin v normotermii, protože po skončení terapeutické hypotermie má většinou pacient sklon k reaktivní hypertermii, která s sebou může přinést velkou řadu komplikací. Velkou výhodou endovaskulárních metod je fakt, že výrazně usnadňují práci ošetřujícímu personálu a umožňují tak soustředit se na další aspekty intenzivní péče o kriticky nemocného. Za nevýhodu mohou někteří považovat vysokou pořizovací cenu přístroje, ale také náklady spojené s provozem (drahé sety, katetr i dražší močový katetr, který je nutností).
Ukončení řízené hypotermie. Plánované ukončení řízené hypotermie se provádí po uplynutí 24 hodin a pacient se kontrolovaně zahřívá. V rámci ohřívání dochází k vazodilataci, a proto pacienta v případě potřeby podporujeme katecholaminy, popř. použijeme volumoterapii. Normotermii udržujeme dalších 48 hodin. Neplánovaně můžeme terapeutickou hypotermii ukončit při zlepšení neurologického nálezu (pacient vyhoví výzvě), v tomto případě nemusíme dodržet 24hodinnový protokol a můžeme začít zahřívat dříve, je ale třeba neurychlovat zahřívání, protože by mohlo dojít ke komplikacím typu bradykardie až zástavy nebo k nežádoucímu závažnému krvácení. Neplánovaně můžeme hypotermii ukončit rovněž při nové přítomnosti vylučovacích kritérií a také při život ohrožující koagulopatii a krvácení.
Sedace. Při terapeutické hypotermii musí být pacient dokonale sedován, protože podchlazení organismu může způsobit třesavku, která produkuje teplo, a také svaly tím mají větší nároky na kyslík. U těchto pacientů podáváme tlumení kontinuálně pomocí lineárních dávkovačů. Používáme opioidní analgetika – Sufenta Forte (sufentanilum) v kombinaci s benzodiazepiny (Midazolam – midazolam-hydrochlorid) nebo Propofol 1% (propofolum), ten však není doporučován u pacientů s prodělaným akutním infarktem myokardu. Propofol má kardiodepresivní účinky. Analgosedace je dávkována individuálně, neboť citlivost na tyto léky je různá. Pokud dochází k třesavce i při kontinuální sedaci, je možné využití svalových relaxancií (Tracrium – atracurium-besylate). Tato dokonalá analgosedace s sebou může přinášet pokles krevního tlaku, a protože je důležité udržovat dostatečnou perfuzi orgánů, udržovat MAP (střední arteriální tlak) nad 65 mm Hg, je výhodou při potřebě použití katecholaminů – Noradrenalin (Norepinefrin-Tartarát), Dopamin (dopamin-hydrochlorid).
Při terapeutické hypotermii udržujeme pacienta v umělém spánku, a proto je třeba komplexní ošetřovatelské péče. Na JIP nebo ARO pacienta kontinuálně monitorujeme a všechna data pravidelně zaznamenáváme do dokumentace. Pečujeme o pacienta jako celek a celkovou hygienu provádíme 2krát denně. Zvláštní péči věnujeme invazivním vstupům, vždy k nim přistupujeme asepticky. Tělesnou teplotu měříme kontinuálně a zaznamenáváme každou hodinu, stejně jako základní životní funkce (IBP – invazivní krevní tlak měřený z arteriálního katetru, EKG, SpO2, CO2, bilanci tekutin). Pacienta pravidelně odsáváme z ETI a udržujeme dýchací cesty průchodné, sledujeme dechovou aktivitu pacienta během řízené ventilace.
Alternativní metody chlazení
Patří mezi ně kombinace zevního a vnitřního chlazení. Shodně se začíná s ochlazením podáním chladného krystaloidního roztoku intravenózně v množství 30 ml/kg o teplotě 4 °C přetlakovou manžetou (maximálně do 60 minut od obnovení vlastního oběhu). Tyto metody nezajišťují pacientovi takový komfort jako metody endovaskulární. Pacient musí být také kvalitně ztlumen.
Fyzikální chlazení – 2 litry chladného krystaloidního roztoku intravenózně, dále podáváme každou hodinu do žaludku cestou NGS (nazogastrická sonda) 150 ml FR zchlazeného na 4 °C. Pacienty obkládáme chladnými gely (nesmí být zmrzlé), které pokládáme do oblastí velkých cév (do oblasti karotid, třísel, na hlavu, popř. na jaterní krajinu). Pokud tato opatření nejsou dostatečná, doplňuje se toto chlazení ještě podáním studeného FR 1/1 o množství 150 ml do močového měchýře cestou PMK každou hodinu. Takto pacienta chladíme 24 hodin a pravidelně sledujeme jeho tělesnou teplotu. Nevýhodou tohoto chlazení je obtížná kontrola a regulovatelnost tělesné teploty, je zde nebezpečí „přechlazení“ a pacient se může dostat do kritické hypotermie, která obnáší mnoho komplikací. Mohou se vyskytnout také místní reakce na přímý kontakt s chladivými gely. Výhodou této metody je, že k chlazení není potřeba zvláštního vybavení, je levná a všem dostupná. I při této metodě je nutné pacienta kontinuálně sedovat a monitorovat. Po uplynutí 24 hodin je vysazováno aktivní chlazení a pacient je postupně ohříván na požadovaných 36,5 °C. V případě nedosažení cílové hypotermie uvedeným způsobem je aktivní ochlazování prováděno 24 hodin a poté ukončeno.
Chladicí obleky a dečky – na některých pracovištích se používají chladicí obleky nebo dečky. Začátek chlazení je v rámci fyzikálního chlazení stejný, provádí se RIVA (rychlá intravenózní aplikace krystaloidního roztoku), dále se pacient balí na 24 hodin do chladicího obleku, ve kterém proudí studená tekutina. Je zde menší možnost místních reakcí na kůži. Chladicí dečky se pokládají pod pacienta a na něj, proudí v nich také chladný roztok, jehož teplota nesmí být nižší než 8 °C. Nutná je kontrola kožního krytu v místech kontaktu s chladicími prostředky.
Komplikace řízené hypotermie
Nejsou časté, můžeme se setkat s krvácením, zejména do gastrointestinálního traktu. Dalšími komplikacemi mohou být poruchy rytmu, zejména bradykardie a snížení srdečního výdeje. Může dojít ke komplikované poruše v iontogramu a rozkolísání vnitřního prostředí. Nutná je pravidelná kontrola laboratorních výsledků, hlavně ionty, ABR (acidobazická rovnováha) a ostatní biochemická a hematologická vyšetření. Můžeme se setkat s infekčními komplikacemi, a to z důvodu imunosupresivního účinku hypotermie, patří sem bakteriémie, pneumonie, tracheobronchitida. K infekčním komplikacím většinou dochází například vlivem předchozí aspirace před endotracheální intubací nebo při ní, anebo při kardiopulmonální resuscitaci. Během RIVA může dojít ke vzniku plicního otoku. Při zevním chlazení může také dojít ke vzniku omrzlin v místě položení chladicích prostředků, zejména u pacientů s chladovou alergií.
Výhody kontrolované normotermie
Udržování normotermie je schopen zajistit pouze endovaskulární systém, přístroj Coolgard. Normotermii udržujeme 48 hodin po zahřátí na požadovanou teplotu 36,5 °C. Tím zabráníme reaktivní hypertermii, která může působit na organismus velmi nepříznivě. U ostatních metod se normotermie udržuje velmi obtížně, a proto hypertermie doprovází velké procento chlazených pacientů. Hypertermie může nastartovat zánětlivou odpověď organismu a s tím související velkou skupinu komplikací, např. ARDS, SIRS, septický stav atd.
Speciální katetr na chlazení k přístroji Coolgard můžeme pacientovi ponechat až 4 dny a poté ho vyjímáme. Před vyjmutím katetru je třeba odpojit přístroj od bočních vstupů, a tím vypustit balónky naplněné fyziologickým roztokem. Odstraníme stehy fixující katetr ke kůži, opatrně vytáhneme katetr a tlakem na místo vpichu tamponujeme preventivně proti krvácení vně i podkožně, přiložíme tlakový obvaz a doporučíme pacientovi, aby alespoň 2 hodiny nehýbal dolní končetinou a měl ji nataženou. Je nutné pravidelně místo vpichu kontrolovat, aby nedošlo k opětovnému krvácení.
Kazuistika
51letý pacient podstoupil kardiopulmonální resuscitaci, PTCA (perkutánní transluminální koronární angioplastika) a následnou terapeutickou hypotermii přístrojem Coolgard, výsledkem je dobrý neurologický nález pacienta.
Anamnéza – z osobní anamnézy máme informace pouze o tom, že prodělal běžná dětská onemocnění a s ničím se neléčí. Jeho rodinná anamnéza je zajímavá, otec i babička zemřeli na akutní infarkt myokardu. Nyní pacient pracuje dlouhodobě v zahraničí a živí se manuální prací. Přiznává 10 cigaret denně, později od manželky, která pracuje jako všeobecná sestra, je získána informace, že pacient je interně zdráv, pouze mu byly naměřeny vyšší hodnoty cholesterolu v krvi, alergii neudává.
Status praesens – pacient udává, že před třemi týdny byl na manipulacích u fyzioterapeuta pro potíže se zablokovanou páteří. Dnes, 9. 12. 2011, při cestě ze zaměstnání, zhruba v 17 hodin, měl náhle pocit na omdlení, horkost v obličeji, pocit pálení žáhy a brnění v levé horní končetině. Dojel domů, tam se najedl a vypil jedno pivo, poté šel spát. Ve 21.30 hodin se probudil s pocitem celkové nevůle a rozhodl se, že si dojede do nemocnice. Sedl do auta a sám jel na interní ambulanci nemocnice v Karlových Varech, kam dorazil ve 22.30 hodin. Pacient subjektivně udává pocit tlaku v epigastriu, pocit tlaku do krku, zažívací potíže neguje, má pocit parestezie v levé horní končetině. Objektivně je orientován místem i časem, spolupracuje, bez dušnosti, krevní tlak má 165/100 mm Hg, puls 70/min. SpO2 98 %. Hlava bez známek zevního traumatu, zornice izokorické, krk zevně bez nálezu, štítná žláza nezvětšena. Hrudník poklepově plný, dýchání sklípkové, akce srdeční pravidelná, břicho měkké, peristaltika slyšitelná, dolní končetiny bez otoků, puls hmatný.
EKG – sinus, frekvence 65/min., elevace ST (úseku EKG křivky ve svodech II, III).
Závěr – akutní infarkt myokardu diafragmatické oblasti, kontaktován kardiolog, podán Kardegic (lysin-acetylsalicylát) 500 mg, Plavix (clopidogreli-sulfas) 75 mg 4 tablety, Heparin (heparinum-natricum) 5 000 j.
Náhle vzniká porucha vědomí, cyanóza, dále progreduje bezvědomí, na monitoru náhlá porucha rytmu – komorová fibrilace, zahájena KPR. Podán Mesocain (Trimecaini-hydrochloridum) 1 amp., Cordarone (amiodaroni hydrochloridum) 1 amp., výboj 1krát defibrilace, poté bradykardie pod 30/min., podán Atropin (atropin-sulfát monohydrát) 0,5 mg 1 amp., dále dle monitoru sinusový rytmus s ojedinělými extrasystolami.
Příchod pracovníků anesteziologicko-resuscitačního oddělení, nalezena cyanóza, neměřitelná saturace, podán Midazolam 5 mg, endotracheální intubace rourkou číslo 8,0, UPV (umělá plicní ventilace) pomocí režimu SIMV (Synchronized Intermittent Mandatory Ventilation – plně řízený ventilační režim), zaveden permanentní močový katetr s teplotním čidlem a podán studený FR o objemu 1 000 ml do periferního žilního katetru. Pacient je odvezen na kardiointervence, kde probíhá 60minutový výkon s nálezem stenózy jednoho segmentu, aplikován jeden stent.
Výkon proběhl bez komplikací, bez nutnosti podání katecholaminů. Během výkonu docházelo ke kašli, ale není validní vědomí. Na ARO se s pacientem přijíždí v 0.40 hodin 10. 12., jsou mu zavedeny invaze – arteriální katetr cestou a. radialis sin., speciální katetr k přístroji Coolgard cestou v. femoralis a NGS. Odebrán kompletní vstupní screening do laboratoře. Probíhá kompletní monitorace a zabezpečování pacienta na lůžku. V 1.00 hodin pacientovi připojen endovaskulární systém na chlazení a ve 2.00 dosaženo cílové teploty 33,5 °C. Kontinuální sedace – Sufenta Forte (sufentanilum) rychlostí 3 ml/hod, Propofol 1% (propofolum) rychlostí 15 ml/hod.
Pacient od příjmu stabilní, bez nutnosti použití katecholaminů, akce srdeční pravidelná, ojediněle komorové extrasystoly, jinak sinusový rytmus. Kontrolní ranní odběry, zde již hodnoty hs (hight-senzitivního) troponinu jsou na nejvyšší hodnotě (2 157). Diuréza je spontánní a dostatečná, ABR bez poruchy pH, fyziologická hodnota laktátu.
V plánu je pokračování v řízené hypotermii po dobu 24 hodin, poté pomalé zahřívání a sledování vědomí pacienta.
11. 12. od 1.00 hodin nastaveno na přístroji Coolgard pomalé zahřívání o 0,5 °C za hodinu. V 7.00 hodin dosaženo cílové normotermie, při ranní vizitě lékaři rozhodli o přepojení pacienta na zástupovou ventilaci pomocí režimu CPAP (Continue Possitive Airway Pressure – režim, který umožňuje pacientovi spontánně dýchat při kontinuálním přetlaku v dýchacích cestách), sníženo množství léků na tlumení. Při spontánní ventilaci přes UPV a plném vědomí bude pokus o extubaci pacienta. Po ranní toaletě je pacient při plném vědomí, špatně tolerující ETI, má stabilní oběh a prognosticky příznivý průběh, to lékaře přesvědčí o extubaci. Pacient je v 10.30 hodin extubován a na několik hodin je mu ponechána kyslíková maska s přívodem kyslíku 4 l/min. Později při stabilizaci oxygenace ponechán pacient bez O2 suplementace.
Pacient je klidný, orientovaný a dobře spolupracuje, subjektivně udává bolesti hrudního koše po KPR, bolest levého ramene při pohybu. Akce srdeční pravidelná, 90/min., IBP (Invasive Blood Pressure – invazivní krevní tlak) 125/80, bez dušnosti, bez přísunu kyslíku má SpO2 hodnotu 94 %. Kolem 13. hodiny obnoven perorální příjem tekutin. Kvůli lepšímu pohybu a komfortu pacienta vytažen katetr k přístroji Coolgard dříve, bez možnosti využití udržování normotermie 48 hodin. Zaveden periferní žilní katetr. Na 12. 12. naplánován překlad na INT JIP.
12. 12. pacient přeložen na interní jednotku intenzivní péče, je stabilní: normotenze, akce srdeční pravidelná, saturace výborná, vědomí na úrovní škály GCS 15 bodů. Močení spontánní, bilance tekutin vyrovnaná. Laboratorní výsledky bez patologických změn.
13. 12. provedeno pacientovi transtorakální ECHO, jehož závěrem je porucha kinetiky posteroseptálně, kde je akinéza, těžká hypokinéza báze spodní stěny, dobrá funkce levé komory, stopové regurgitace na A-V úsecích. V 15.00 je pacient přeložen na standardní interní oddělení, kde je hospitalizován do 15. 12. a poté je propuštěn do domácího léčení. Je mu doporučena kontrola do tří dnů u praktického lékaře s kontrolou krevního tlaku a eventuální úpravou případné hypertenze. Dále bude sledován kardiologem. Pro bolesti a pocit parestezie levé horní končetiny je pacient doporučen na neurologické vyšetření. V propouštěcí zprávě je doporučena kontrola lipidogramu, dodržování racionální výživy, nízkocholesterolové diety, zvýšení fyzické aktivity a odstranění kuřáckých návyků.
Pacient je poučen o nutnosti dodržovat předepsanou medikaci – Trombex (clopidogreli sulfas) 75 mg 1-0-0 po dobu 12 měsíců, Anopyrin (kyselina acetylsalicylová) 100 mg 0-1-0 (doživotně), Lescol XL (fluvastatinum natricum) 0-0-1, Prestarium NEO (perindoprilum argininum) 1-0-0, Concor 2,5 (bisoprololi fumaras) 0-0-1, Controloc 20 (pantoprazolum natricum sesquihydricum) 0-0-1.
Při rychlé a odborné resuscitaci nedošlo k hypoxii tkání, a proto pacientův neurologický nález je bez patologických změn. PTCA proběhlo bezodkladně, a proto došlo k rychlému zprůchodnění postižené koronární tepny. Došlo k využití všech dosažitelných možností léčby, pacient byl hospitalizován po KPR pouhých 6 dní.
Terapeutická hypotermie z velké části zabrání vzniku poresuscitační nemoci, která bezpochyby zhoršuje prognózu pacienta po kardiopulmonální resuscitaci.
Na jednotkách intenzivní péče a anesteziologicko-resuscitačních odděleních, která zajišťují poresuscitační péči, by měly být vytvořeny protokoly na terapeutickou hypotermii.
Diskuse a závěr
Na anesteziologicko-resuscitačních odděleních nebo jednotkách intenzivní péče je doporučeno vytvoření protokolu pro řízenou hypotermii, ale také důkladná edukace personálu k této metodě. Doporučuje se začít s chlazením pacienta co nejdříve, a proto by bylo velkým přínosem vytvoření protokolu a dovybavení vozů zdravotnických záchranných služeb pro terapeutickou hypotermii.
Pacient po KPR je ohrožen v mnoha směrech, zejména poresuscitační nemocí, která ho ohrožuje na životě ještě v několika dalších hodinách po resuscitaci. Terapeutická hypotermie při včasném zavedení z velké části zabrání posthypoxickému poškození orgánů, a tím také rozvoji této komplikace. Povšechná ischemie během oběhové zástavy může vést k aktivaci celé řady patofyziologických procesů, které mohou způsobit další, často fatální poškození. Včasná terapeutická hypotermie může zabránit z velké části rozvoji těchto procesů a měla by být již standardním výkonem v intenzivní péči.
Intranazální systém ochlazování
Zdroj: Fotoarchiv firmy Benechill (http://www.puro-klima.cz)

Katetr zavedený do v. femoralis
Zdroj: Fotoarchiv firmy Medial, 2009

Přístroj Coolgard připojený ke katetru
Zdroj: Fotoarchiv firmy Medial, 2009

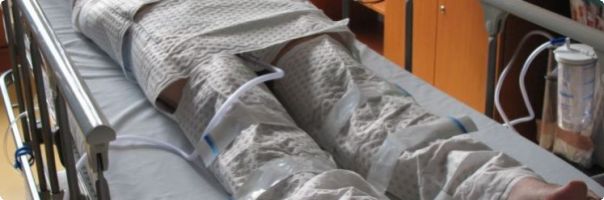
Pacient v chladicím obleku
Zdroj: Fotoarchiv ARO nemocnice Karlovy Vary, 2008

Snímek pořízený při katetrizaci
Zdroj: Fotoarchiv kardiologického oddělení nemocnice Karlovy Vary, 2011
Literatura:
Dostál P. Řízená hypotermie v intenzivní péči – praktické provedení. [cit. 2008-11-4]. Dostupné na http://www.polymed.cz/cms/pdfs/MEDVision_MUDr_Dostal.pdf
Dostál P, Černý V, Cvachovec K et al. Anesteziologie a intenzivní medicína. Praha, 2009. [cit. 2009-05-18]. Dostupné na http://www.prolekare.cz/anesteziologie-intenzivni-medicina-clanek/konsenzualni-stanovisko-k-pouziti-terapeuticke-hypotermie. ISSN 1803-6597.
Ošťádal P, Janotka M et al. Zdravotnické noviny. Praha, 2009. [cit. 2009-11-6]. Dostupné na http://www.zdn.cz/clanek/postgradualni-medicina/endovaskularni-rizena-hypotermie-u-nemocnych-po-srdecni-zastave-448001. ISSN 1214-7664.
Puroklima. 2011. Přístroj RhinoChill. Dostupné na http://www.puro-klima.cz/CZ/406/rhinochill%20/.
Sýkora R. Vnitřní lékařství. Praha, 2011. [cit. 2011-01-12]. Dostupné na http://www.vnitrnilekarstvi.cz/vnitrni-lekarstvi-clanek/infekcni-komplikace-u-pacientu-po-srdecni-zastave-pri-terapeuticke-hypotermii. ISSN 1801–7592.
Recenzovaly:
Mgr. Alena Chmaitilliová, II. chirurgická klinika kardiovaskulární chirurgie 1. LF UK a VFN, Praha, vrchní sestra
Hana Fišerová, Interní kardiologická klinika FN Brno, vrchní sestra
Literatura:
Dostál P. 2008. Řízená hypotermie v intenzivní péči – praktické provedení. [cit. 2008-11-4]. Dostupné na http://www.polymed.cz/cms/pdfs/MEDVision_MUDr_Dostal.pdf
Dostál P, Černý V, Cvachovec K et al., 2009) Anesteziologie a intenzivní medicína. Praha, 2009. [cit. 2009-05-18]. Dostupné na http://www.prolekare.cz/anesteziologie-intenzivni-medicina-clanek/konsenzualni-stanovisko-k-pouziti-terapeuticke-hypotermie. ISSN 1803-6597.
Ošťádal P, Janotka M et al. Zdravotnické noviny. Praha, 2009. [cit. 2009-11-6]. Dostupné na http://www.zdn.cz/clanek/postgradualni-medicina/endovaskularni-rizena-hypotermie-u-nemocnych-po-srdecni-zastave-448001. ISSN 1214-7664.
Puroklima. 2011. Přístroj RhinoChill. Dostupné na http://www.puro-klima.cz/CZ/406/rhinochill%20/.
Sýkora R. Vnitřní lékařství. Praha, 2011. [cit. 2011-01-12]. Dostupné na http://www.vnitrnilekarstvi.cz/vnitrni-lekarstvi-clanek/infekcni-komplikace-u-pacientu-po-srdecni-zastave-pri-terapeuticke-hypotermii. ISSN 1801–7592.
Recenzovaly:
Mgr. Alena Chmaitilliová, II. chirurgická klinika kardiovaskulární chirurgie 1. LF UK a VFN, Praha, vrchní sestra
Hana Fišerová, Interní kardiologická klinika FN Brno, vrchní sestra
Nikola Brizgalová, DiS. KKN Karlovy Vary, ARO – lůžková část
Další články v tomto čísle
- Čas odhalí pravdu
- Informujeme - Vítejte ve starých časech
- Rozhovor s Lenkou Gutovou: „Chybám se snažíme předcházet“
- Doporučené postupy k odběrům krve – prevence preanalytické variability
- Dezinfekce v ambulantní praxi
- Z praxe zkušené stomasestry (III. díl)
- Prevence rakoviny varlat u mužů v reprodukčním věku
- Posudzovanie kognitívnych porúch u seniorov
- Jak pečovat o diabetickou nohu
- Kolorektální karcinom – screening imunochemickou metodou v ordinaci praktického lékaře